Lab № reacții de culoare 7 proprietăți de proteine pentru proteine și aminoacizi
Reacții de culoare pentru proteine Experiment 1. Reacția biuret.
reacție Biuretul - calitate pentru toți, fără excepție proteine. și produsele de hidroliză parțială a acestora. care conțin cel puțin două legături peptidice.
Principiul metodei. reacția de biuret datorită prezenței legăturilor peptidice în proteine (- CO - NH -), care, într-un mediu alcalin pentru a forma un sulfat de cupru (II), vopsite în complexe de sare cum ar fi culoarea de cupru roșu-violet. reacția biuret oferă unele substanțe neproteice, cum ar fi biuret (NH2-CO-NH-CO-NH2), oxamidă (NH2 CO-CO-NH2), un număr de aminoacizi (histidină. Serina. treonină. asparagină).
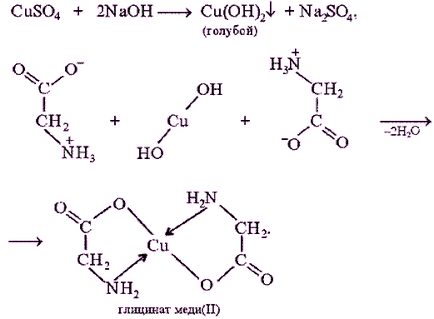
reacția biuret cu glicină
Ordinea de performanță.
La 1 ml de soluție de proteină de 1% a fost adăugat un volum egal de soluție de hidroxid de sodiu 10% (NaOH) alcalin și apoi 2-3 picături de soluție 1% de sulfat de cupru (CuSO4). dilua, soluție aproape incoloră de sulfat de cupru.
Când o reacție pozitivă apare de culoare violet, cu o tentă roșie sau albastră.
Experiența 2.Reaktsiyana „slab cuplate sulf.“
Principiul metodei. Aceasta este o reacție la cisteina și cistina. Hidroliza alcalină „sulf slab cuplate“ în cisteină și cistină destul de ușor scindate, formând astfel hidrogen sulfurat, care reacționează cu alcalii dă sodiu sau potasiu sulfurat. Prin adăugarea de acetat de plumb (II) format precipitat de sulfură de plumb (II) un gri-negru.
Ordinea de performanță.
Tubul se toarnă 1 ml proteină de pui nediluat se adaugă 2 ml de soluție de hidroxid de sodiu 20%. Amestecul a fost încălzit ușor (la amestec este aruncat).
Aceasta eliberează amoniac, care este detectată de hârtie de turnesol umed albăstreală pentru rufe, badged la deschiderea tuburilor (nu atinge peretii). Precipitatul rezultat este dizolvat cu reflux ușor și apoi se adaugă 0,5 ml dintr-o soluție de acetat de plumb (II). Există o pierdere de gri-negru precipitat plumb sulfură (II):
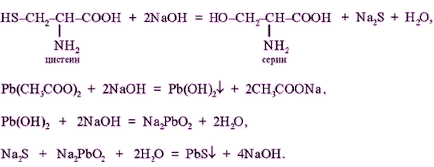
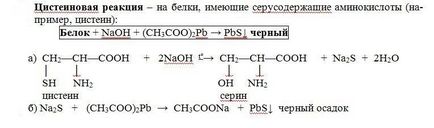
Țeava de turnare 1 ml. proteine de pui nediluat se adaugă 2 ml. soluție alcalină concentrată, pune mai multe refierbătoare. La soluția fierbinte s-a adăugat o soluție de plumbite de sodiu - format o culoare galben-maro sau negru. (Sodiu Plyumbit preparat după cum urmează: a 1 ml de soluție de acetat de plumb alcalină s-a adăugat în picături până la dizolvare care formează inițial un precipitat de hidroxid de plumb).
În prezența aminoacizilor sulfului acizilor din molecula de proteină (cistină, cisteină) a acestor aminoacizi este clivat treptat sulf sub forma unui ion în starea de oxidare - 2, a cărei prezență este detectată și ion de plumb, ion de sulf care formează sulfura de plumb insolubil, negru:
Pb (CH3 COO) 2 + 2NaOH Pb (OH) 2 + 2 CH3 COONa,
Pb (OH) 2 + 2NaOH + Na2 PbO2 H2O,
Na2S + Na2 PbO2 + 2H2O PbS + 4NaOH.
A face experiența: pentru a trage o concluzie și scrie ecuația reacției.
3. Experiența ksantoproteinovaya proteine de raspuns.
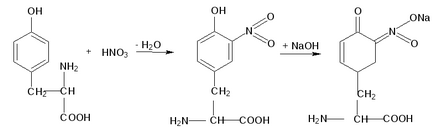
Principiul metodei. Această reacție este utilizată pentru detectarea unui-aminoacizi care conțin radicali aromatici. Tirozină, triptofan, fenilalanină prin reacția cu acid azotic concentrat, pentru a forma nitro derivați având o colorație galbenă. Într-un mediu alcalin, acești derivați nitro ai-aminoacizilor da săruri, vopsite în culoarea portocalie. Gelatina, de exemplu, nu conține aminoacizi aromatici, nu proba ksantoproteinovaya.
Ordinea de performanță.
La 1 ml de 10% ou se adaugă 0,5 ml de soluție concentrată de proteină de acid azotic. Ca rezultat, coagularea proteinelor, un precipitat alb sau turbiditate în conținutul tubului. După încălzirea soluției și precipitatul este colorat într-o culoare galben strălucitor. In acest precipitat aproape complet dizolvat în hidroliză. După răcire, 2,1 ml de soluție de hidroxid de sodiu 20% (până când culoarea portocalie a soluției).
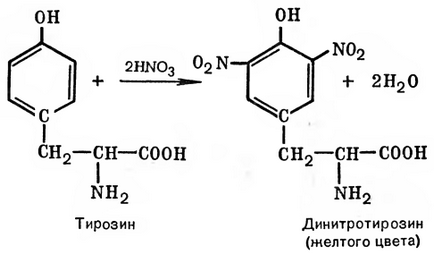
Să luăm în considerare mecanismul reacției de tirozină ksantoproteinovaya radicală:
Să luăm în considerare mecanismul reacției de tirozină ksantoproteinovaya radicală:
Produs de condensare albastru-violet
Reacția cu ninhidrină este utilizat pentru detectarea vizuală a-aminoacizi în cromatograma (hârtie, în strat subțire), și, de asemenea, pentru determinarea colorimetrică a concentrației de aminoacizi din intensitatea colorației produsului de reacție.
Produsul din această reacție conține în componența sa un radical (R) al aminoacidului inițial, care determină diferite culori: albastru, roșu, etc. Compușii care rezultă din reacțiile de aminoacizi cu ninhidrină.
În prezent, reacția ninhidrină este larg utilizat pentru deschiderea de aminoacizi individuali, și pentru a determina valoarea lor.
Ordinea de performanță.
Țeava de turnare 1 ml de soluție diluată de tărie 1,10% din ou de pui alb, și 2,1 ml dintr-o soluție 1% de ninhidrină în acetonă. Conținutul tubului de testare și se agită timp de 2-3 minute încălzite ușor într-o baie de apă până când culoarea albastru-violet, indicând prezența a-aminoacizi în proteină.
A face experiența: pentru a trage o concluzie și scrie ecuația reacției.
6. Experiența de reacție Sakaguchi.
Principiul metodei. Această reacție asupra arginina de aminoacizi se bazează pe interacțiunea argininei cu-naftol, în prezența unui oxidant. Mecanismul său nu este încă pe deplin înțeles. Aparent, reacția se realizează conform următoarei ecuații:
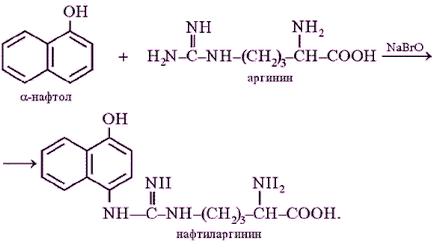
Deoarece derivații de quinonic (în acest caz naftochinonă), în care hidrogenul din grupa imino -NH- este înlocuit cu un radical alchil sau arii, colorate întotdeauna în culorile galben și roșu, se pare a fi de culoare portocalie-roșie a soluției în timpul reacției datorită apariției Sakaguchi și anume derivat naftohinonimina. Nu este exclus, cu toate acestea, probabilitatea de formare a mai compus complex datorită oxidării în continuare a NH-gruparea rămasă a restului de arginină și inelul benzenic a-naftol:
Ordinea de performanță.
La 2 ml. 1% soluție diluată de proteine de ou de pui se adaugă 2 ml. 10% hidroxid de sodiu (NaOH) și câteva picături de soluție alcoolică 0,2% α-naftol. Conținutul tuburilor amestecate bine. Apoi se toarnă 0,5 ml. hipobromit de sodiu (NaBrO) sau hipoclorit de sodiu (hipoclorit de sodiu - NaOCI), se agită. Imediat se pare colorare roșu, crescând treptat.
Se adaugă imediat 1 ml dintr-o soluție 40% de uree pentru a stabiliza rapid dezvolta o culoare roșu-portocaliu.
Acest răspuns este caracteristic compușilor conținând reziduul de guanidină
și indică prezența unei molecule de proteine, aminoacizi-arginina:
NH = C -NH - (CH2) 3-CH-COOH