Structura lanțului polipeptidic și legătura peptidică
monomeri aminoacizi, care fac parte din polipeptide, resturile de aminoacizi menționate. rest de aminoacid care are o grupare amino liberă, numită N-terminal și înregistrate în partea stângă a lanțului peptidic și având un grup liber α-carbo-ksilnuyu - C-terminal, și este înregistrată pe dreapta. Intervalul acestui circuit repetă atomi-CH - CO - NH- în polipetidnoy lanț numita peptidă coloana vertebrală.
Lanțul polipeptidic are următoarea formă generală:
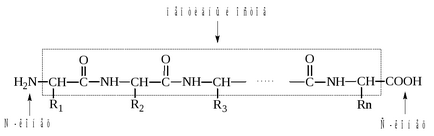
în care R1. R2. R3. ... Rn - radicali de aminoacizi care formează catena laterală.
În manifestarea funcțiilor biologice ale peptidelor și proteinelor joacă un rol important structurii electronice și spațială a grupului de peptide:
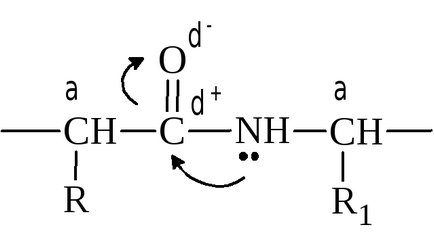
Prezența grupării p-π-conjugare în peptidă conduce la obligațiuni dvoesvyazannosti parțială - N. Lungimea legăturii peptidice C - N este egal cu 0,132 nm și lungimea legăturii N - Sα este 0.147 nm. Legătură simplă C - N, în peptidele din aproximativ 40% are natura legăturii duble și dubla legătură C = O la aproximativ 40% este unică. Acest fapt are două consecințe importante:
1) o grupare imino (- NH -) o legătură peptidică are abilitatea de a scinda sau atașa un proton pronunțat nu semnificativ;
2) rotația liberă în jurul legăturii C - N offline.
Parțială dvoesvyazannost C - N înseamnă că fragmentul peptidic este o porțiune plană a lanțului peptidic. grupări Peptide plane dispuse la un unghi față de celălalt:
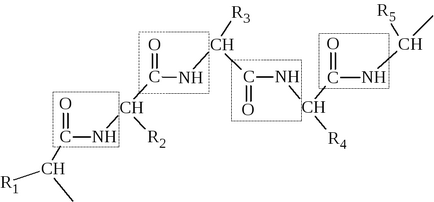
In jurul C - Sα și a N - Sα posibilă rotație, deși limitată ca mărime și natura radicalilor, permițând lanțurile polipeptidice să ia o varietate de configurații.
Legătura peptidică este o legătură covalentă simplă, prin care resturile de aminoacid conectate între ele, care formează scheletul moleculei de proteină.
Legăturile peptidice sunt în general situate într-o configurație trans, adică α-carbon atomii sunt situate pe fiecare parte a legăturii peptidice. Ca rezultat, grupările laterale de aminoacizi sunt în spațiul la cea mai mare distanță unul față de celălalt.
peptide Homenklatura
Când titlul polipeptidic la numele tuturor resturilor de aminoacizi cu excepția ultimului, adăugați sufixul -il. aminoterminal se termină cu -in. De exemplu, peptida Met-Asp-Val-Pro este numele complet al aspartil metionil turnat prolină.
Proprietățile acide ale peptidelor
Multe peptide scurte au fost obținute în cristal-cristal forma pura. Temperatura ridicată a punctului de topire la cea a peptidelor soluții neutre cristalizează ca ioni bipolari. Deoarece nici una dintre grupările oc-carboxil, și nici unul dintre grupurile oc-amino sunt implicate în formarea legăturilor peptidice, nu pot fi ionizate în intervalul de pH la 0 la 14, proprietățile acide ale peptidelor sunt determinate de gruparea NH2 liber de rest N-terminal și o grupare carboxil liberă reziduu C-terminal al peptidei și acele grupări R care sunt capabile de ionizare. Numărul de lanțuri de peptide lungi ionizate R-grupuri sunt de obicei mari în comparație cu cele două grupe de capăt ionizat resturile peptidice. Prin urmare, pentru a caracteriza proprietățile acide ale peptidelor, vom considera peptide scurte.
Liberă α-amino și gruparea carboxil terminală liberă în peptidele separate printr-o distanță semnificativ mai mare decât simpli aminoacizi, și, prin urmare, electrostatic inter-acțiune a slăbit între acestea. Valorile PK ale grupărilor terminale carboxil din peptide este puțin mai mare și la gruparea amino-terminală α este mai mică decât în aminoacizii liberi corespunzători. In R grupurile nu diferă în mod semnificativ în peptide și aminoacizi liberi în valorile pK respective.
Pentru a defini intervalul de pH în care punctul izoelectric poate fi o peptidă scurtă test, este suficient pentru a compara numărul de grupări amino libere și numărul de grupări carboxil libere, inclusiv N- și grupări C-terminale. Dacă numărul de grupe amino depășește numărul de grupe carboxil izoelektri Env punct peptid se va afla în regiunea de pH alcalin, pentru a preveni protonarea grupărilor amino necesare alcaline. Dacă numărul de grupe carboxil depășește numărul de grupări amino, punctul izoelectric va fi în intervalul de pH acid, deoarece mediul de acid inhibă disocierea grupărilor carboxil.