Substanțe simple și complexe
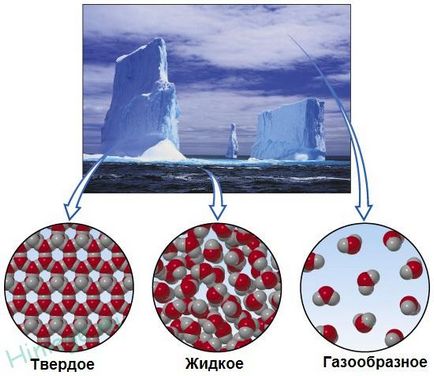
Trei stări agregate de apă
Lumea din jurul nostru este un material. Problema este de două feluri: materia și câmp. chimia obiect - substanța (inclusiv efectul asupra diferitelor domenii ale substanței - acustice, magnetice, electromagnetice etc.).
Agent - toate că masa de repaus (adică, caracterizată prin masă atunci când nu este în mișcare). Astfel, deși o singură masă de repaus de electroni (masa nu se deplasează de electroni) este foarte mic - aproximativ 10 -27 g, dar chiar și un electron - această substanță.
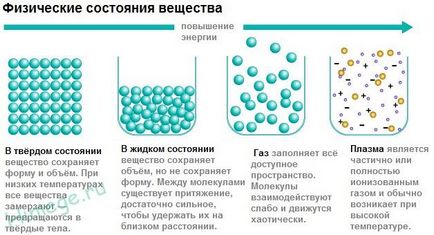
Substanța este în trei stări - gazoase, lichide și solide. Mai există o stare a materiei - plasmă (de exemplu, plasma este în furtună și fulger globular), dar în cursul școală de chimie plasmă nu este aproape considerat.
Substanțele pot fi curate, foarte curat (dreapta, de exemplu, pentru a crea o fibră optică) poate conține cantități apreciabile de impurități pot fi amestecuri.
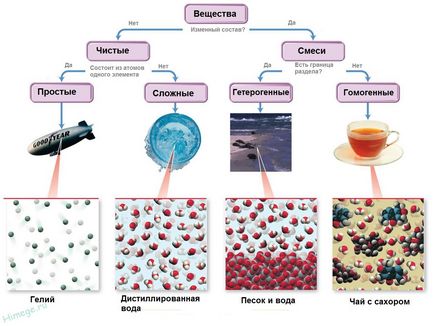
Toate substanțele constau din particule minuscule - atomi. Substanțele care constau dintr-un tip de atomi (atomi de un element) sunt numite simplu (de exemplu, cărbune, oxigen, azot, argint și altele.). Substanțele care conțin atomi interconectate de elemente diferite, numite complexe.
Dacă există două sau mai multe substanțe simple și atomii lor nu sunt legați, este menționată nu complex, și un amestec de substanțe simple într-o substanță (de exemplu, aer). Numărul de substanțe simple, este relativ mică (aproximativ cinci sute), iar numărul de compuși complecși este enormă. Până în prezent, zeci cunoscute de milioane de substanțe diferite complicate.
Substanțe capabile intră în angrenare una cu cealaltă, și există substanțe noi. O astfel de conversie chimică se numește. De exemplu, simplu carbon substanță este reacționată (chimiști - reacționat vorbit) cu o altă substanță simplă - oxigen, rezultatul este un complex de substanță - dioxid de carbon, în care atomii de carbon și oxigen sunt legați. Astfel de transformări sunt unele substanțe alte substanțe chimice numite. Transformările chimice - o reacție chimică. Astfel, atunci când este încălzit în aer complex îndulcitor de zahăr - zaharoză (care constă din zahăr) - se transformă într-o substanță simplă - carbon și substanță complexă - apă.
Transformarea Studii chimice ale altor substanțe. Vizați chimie - afla ce substanta poate interacționa (răspunde) unei substanțe în aceste condiții, care este astfel formată. În plus, este important să se determine în ce condiții poate să apară sau că conversia și substanța dorită poate fi obținută.
Fiecare substanță este caracterizată printr-un set de proprietăți fizice și chimice. Proprietăți fizice - sunt proprietăți care pot fi descrise cu ajutorul unor dispozitive fizice. De exemplu, un termometru poate determina temperatura de topire și apa de fierbere. Metodele fizice pot fi caracterizate prin capacitatea unei substanțe de a conduce curentul electric, pentru a determina densitatea substanței, duritatea sa, etc. În cazul în care procesele fizice ale materiei rămâne neschimbată în compoziție.
Proprietățile fizice ale substanțelor sunt împărțite în schislimye (cele care pot fi caracterizate prin diverse dispozitive fizice, inclusiv, de exemplu, indicând densitatea, punctele de topire și de fierbere, solubilitatea în apă, și altele.) Și neschislimye (cele care sunt caracterizate de numărul imposibil sau foarte dificil - cum ar fi culoare, miros, gust, etc) ..
Proprietățile chimice ale substanței - este un set de informații despre alte substanțe, precum și condițiile în care intră în interacțiune chimică a substanței. Cea mai importantă sarcină a chimiei - identificarea proprietăților chimice ale substanțelor.
Transformările chimice implicate particule infime de substanțe - atomi. Când se formează în loc transformări chimice ale unor substanțe se formează alte substanțe, iar materiile prime dispar și noi substanțe (produse de reacție). Un atomi în toate reacțiile chimice sunt stocate. Este rearanjarea lor în transformarea chimică a vechilor obligațiuni între atomii sunt distruse, și noi conexiuni.
Numărul de diferite substanțe este enormă (și fiecare dintre ele are propriul set de proprietăți fizice și chimice). Atomii, care diferă una de cealaltă pe cele mai importante caracteristici ale lumii materiale din jur este relativ mic - aproximativ o sută. Fiecare tip corespunde unui atomi de elemente chimice. Element chimic - o colecție de atomi cu aceleași sau caracteristici similare. În natură, există aproximativ 90 de elemente chimice diferite. Pana in prezent, fizicienii au învățat să creeze altele noi, care nu sunt pe pământ tipuri de atomi. Astfel de atomi (și, în consecință, aceste substanțe chimice) numite artificiale (în limba engleză - elemente sintetice sau artificiale). Artificial elemente obținute până în prezent sintetizat mai mult de două duzini.
Fiecare element are un nume latin și un simbol una sau două litere. În limba rusă literatura chimică, nu există reguli clare de pronunție simboluri ale elementelor chimice. Unii pronunțată ca: element rusesc (simboluri de sodiu, magneziu etc.), altele numesc - prin litere latine (simboluri de carbon, fosfor, sulf), și altele - numele sunetului în elementul latin (fier, argint, aur, mercur ). hidrogen simbol element de N am decis să rostească ca scrisoarea este pronunțată în franceză.
Comparația dintre caracteristicile majore ale elementelor chimice și a substanțelor simple, prezentate în tabelul de mai jos. Un element poate întâlni câteva substanțe simple (fenomen: aceste forme alotropice de carbon, oxigen, etc.), dar poate - și una (argon si alte gaze inerte.).
X și m e și h la k și d e l e m e n t
Exemplul C o m e în e o f o m pe