Toți atomii de 1
Numărul de protoni din nucleul atomului celulei strict determinată (egal cu numărul ordinal al elementului din Z periodic). Numărul de neutroni în nucleul atomului și unul elemntov togozhe poate fi diferit (egal cu A - Z, în care A - element de masă atomică relativă, Z - numărul de serie).
Taxa este determinată de sarcina nucleului atomic de protoni.
nucleul atomic de masă este suma maselor de protoni și neutroni.
Izotopi - o varietate de atomi ai unui element având odnakovoe numărul de protoni și un număr diferit de neutroni (atomi diferiți nucleu de masă).
"Izosov" (Gr.) - unul
"Topos" (Gr.) - asezare
Ocupând una (celula) în tabelul periodic D. I. Mendeleeva.
Stony 1891. Energia electrică este transferată la cele mai mici particule care există în atomii tuturor elementelor. Stony numit această particulă "electroni" ( "electron" (greacă) - chihlimbar)).
D. Thompson și G. Perrin Câțiva ani mai târziu a constatat că electronii transporta o sarcină negativă.
D. Thomson a identificat viteza și masa electronului.
Electron - o particulă încărcată negativ.
sarcina sa este numeric egal, dar în semn opus taxa de protoni (-1). Masa sa este foarte mică, și este aproximativ egal cu 1/1840. E. M (9; 109 * 0 000000000000000000000000001 grame)..
Oboznachaetsya
Numărul de electroni într-un atom este egal cu numărul de protoni.
(Determinată de numărul ordinal al elementului din tabelul periodic D. I. Mendeleeva)
In 1924, Lui De Broglie a stabilit natura duală a electronilor - undă și particulă
Mișcarea electronilor în atomi
„Poate că, acești electroni -
Lumi, unde cinci continente.
De artă, cunoștințe, războaie, tronuri
Și amintirea patruzeci de secole.
Mai probabil fiecare atom -
Universul, în cazul în care o sută de planete;
E totul aici, comprimat în volum,
Dar este, de asemenea, ceva care nu este aici. "
(Bryusov, 1922)
mișcarea unui electron dintr-un atom se supune legilor mecanicii cuantice. Ele nu permit interpretarea.
Cu ajutorul dispozitivelor putem observa nu electronul, iar rezultatul interacțiunii sale cu materia.
Ossobennosti mișcarea de electroni din atomul permit să ia în considerare modul în care fiecare mokrooblako de electroni care nu are limite exterioare clare.
Spațiul în care se mișcă de electroni, numit orbital
Probabilitatea de a găsi un electron în orbita descrie densitatea de electroni.
coajă de electroni atomic
Norii de electroni cu energie de electroni similare de cost convingătoare într-un strat atom (nivelul de energie).
Acesta caracterizează nivelul de energie al unei energii de legare de electroni a nucleului. Notat˘a prin cifre arabe (1, 2, 3, 4).
Electronii același nivel macrobiotic poate razlichatsya valori de energie, pentru a forma subnivele de energie. Desemnate prin literele s, p, d, f.
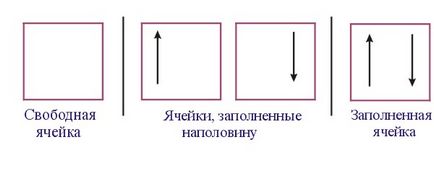
Fiecare nivel (cu excepția lui s) este conținut diferit de mai multe orientate în spațiu orbitali. Diagramele sunt indicate sub forma celulelor cuantice.